В этой статье разберем, как связаны наследственность и рак. И нужно ли искать наследственную предрасположенность к онкологическим заболеваниям.
Рак – следствие мутаций или так называемых поломок в генах. А гены человек получает от своих родителей. Значит ли это, что онкологические заболевания родителей, бабушек и дедушек перейдут к детям вместе с такими поломанными генами?
Отчасти да, ведь около 10% всех онкологических заболеваний наследственные. Но большинство опухолей возникают всё же из-за случайных генетических мутаций, которые накапливаются в процессе жизни. Такие мутации человек не наследует от родных.
Но ведь точно известно, что если у родных был рак, то вероятность его возникновения у потомков существенно увеличивается? Или нет?
Содержание
- Как наследственность связана с раком?
- Что проверить, чтобы понять свои риски?
- Какие тесты помогают выявить риск рака?
- Кому будет полезен генетический тест?
- Что еще можно узнать о раке из генетического теста?
Как наследственность связана с раком?
Онкологические заболевания, злокачественные опухоли или просто рак – это скопления перерожденных или злокачественных клеток, которые бесконтрольно делятся и растут. Нормальные или здоровые клетки перерождаются в злокачественные из-за случайных мутаций в генах.
Среди основных причин, которые запускают генетические изменения, выделяют в первую очередь достаточно распространенные и всем известные факторы, такие как курение, ожирение, солнечное излучение, злоупотребление алкоголем, факторы окружающей среды и некоторые инфекции.
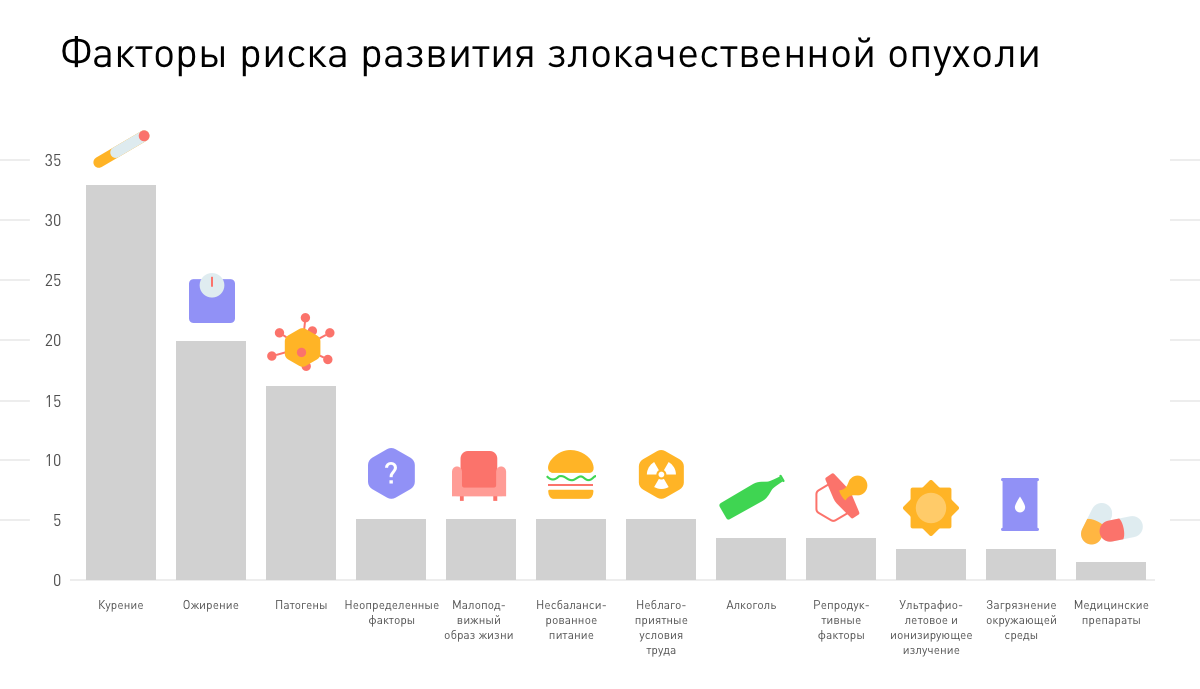
А если заболевание возникло из-за одного из этих факторов, то мутации, спровоцировавшие болезнь, скорее всего, не будут переданы потомкам. Онкологические заболевания, которые возникают в результате приобретенных мутаций, называют спорадическими формами рака.
По статистике, на долю спорадических форм рака приходится около 80% всех случаев онкологических заболеваний.
Но некоторые люди действительно имеют повышенный риск возникновения онкологических заболеваний как раз из-за генетических поломок, которые они получили по наследству от родителей.
Например, человек может получить «в наследство» так называемые дефектные гены, которые отвечают за важные процессы клеточной регенерации. В норме они должны устранять генетические ошибки. Но если ген сломан, ошибки продолжают накапливаться. Хотя даже в этом случае вероятность возникновения заболевания всё равно не 100%.
Самые распространенные наследуемые формы рака: рак желудка, поджелудочной железы, яичников, молочной железы, колоректальный рак и меланома.
Что проверить, чтобы понять свои риски?
Специально искать наследственную предрасположенность к онкологическим заболеваниям и проходить все возможные чекапы и обследования точно не стоит. Но нужно очень внимательно относится к наследственным факторам риска.
Есть ряд признаков, наличие которых по данным Американского общества клинической онкологии (ASCO) должно насторожить:
- У родственников диагностировали рак в возрасте до 50 лет (особенно если это рак молочной железы, яичников или эндометрия, рак простаты, поджелудочной железы или колоректальный рак)
- У двух и более родственников по одной линии (материнской или отцовской) было выявлено онкологическое заболевание
- У родственников был обнаружен тип опухоли или разные опухоли, которые характерны для одного наследственного синдрома
- Несколько форм рака у одного из родных
- У близкого родственника выявлена патогенная наследственная мутация
Если вы отметили у себя хотя бы один из перечисленных пунктов, то, возможно, вы входите в группу высокого риска. В таком случае вам действительно может быть рекомендовано пройти ряд обследований и лабораторных тестов, которые помогут понять, не болеете ли вы сейчас и каков ваш риск заболеть вообще.
Кроме этого, если у человека уже было диагностировано онкологическое заболевание, по некоторым факторам можно заподозрить его наследственную природу:
- Несколько случаев онкологического заболевания в анамнезе
- Болезнь началась на 10-15 лет раньше, чем это характерно для нее в общей популяции
- Первично-множественный рак, когда злокачественные опухоли развиваются одновременно в двух и более органах
Повышенный риск развития онкологических заболеваний передается вместе с генетической мутацией от родителей к детям. Это называется наследственный онкологический синдром.
Чтобы определить риск развития рака в будущем человеку могут предложить пройти генетическое тестирование. Одна из целей такого исследования – выявить унаследованные мутации, чтобы по возможности предотвратить развитие заболевания.
Необходимость проведения такого исследования стоит обсудить со своим лечащим врачом или врачом-генетиком.
Какие тесты помогают выявить риск рака?
В зависимости от метода, которым будут выполнять генетическое исследование выделяют ПЦР, NGS-исследования (Next generation sequencing) и микрочипы.
ПЦР
Чаще всего для выявления клинически значимых мутаций используют ПЦР-исследование. Именно оно входит в большинство клинических рекомендаций и протоколов лечения, утвержденных в России. Программы по выявлению онкорисков, которые предлагают частные клиники и лаборатории, также в основном выявляют патогенные мутации с помощью ПЦР.
Проблема ПЦР-исследований в низкой информативности. Они могут быть использованы для скрининга и позволяют определить не более 10 наиболее частых мутаций. Этого может быть недостаточно, потому что причиной наследственного онкологического синдрома могут выступать более редкие мутации или мутации в других генах.
Выбор в пользу ПЦР обусловлен простотой исполнения и достаточно низкой стоимостью. На этом плюсы заканчиваются.
NGS-исследования
NGS-исследование или высокопроизводительное секвенирование нового поколения – это более углубленное исследование. Оно позволяет массово одновременно секвенировать тысячи фрагментов ДНК. Благодаря этому можно определить 100% мутаций в большом количестве генов.
Например, методом NGS можно выявить патогенные мутации в генах BRCA1/2. Они ассоциированы с высоким риском развития рака груди и яичников. NGS выявляет их у вдвое большего количества пациентов, чем ПЦР. ПЦР выявляет только 5-8 наиболее частых мутаций, при этом, более 15% мутаций высокого риска остаются невыявленными.
Основной минус NGS – высокая стоимость. Но и информативность исследований, выполненных с его помощью, не менее высока.
- Полное секвенирование генома
Дает максимально полные сведения о структуре генетического материала, потому что исследует весь набор генов конкретного человека. Сюда попадут все найденные генетические мутации, в том числе те, в отношении которых пока нет научно-обоснованных связей с развитием заболеваний.
По результатам такого исследования можно оценить предрасположенность к наследственным онкологическим синдромам. А также увидеть патогенные наследственные мутации, которые появились в роду впервые.
Такое исследование проводят, когда есть подозрение на наследственное заболевание, а также если другие методы диагностики оказались неэффективны.
- Исследование экзома
Считается, что более 80% отклонений, которые становятся причиной возникновения заболеваний, происходят в 1% генома. Поэтому исследование этой части генома дает возможность выявить пациентов с высоким риском развития онкологических заболеваний.
В ходе дальнейших исследований можно точечно подтвердить найденные отклонения с высоким риском у самого пациента и его родственников.
Исследования генома и экзома позволяют обновлять данные по мере появления новой информации. Например, когда ученые доказали связь определенной генетической мутации с развитием болезни через несколько лет после того, как человек сдал тест.
- Таргетные панели генов
Такие панели разработаны для различных групп заболеваний, в том числе онкологических. Например, есть панели для рака желудка или рака груди. Они позволяют исследовать определенные гены, мутации в которых связаны с развитием заболеваний.
Сложность с такими панелями в том, что информация о выбранном наборе генов меняется ежегодно. Какие-то данные устаревают, а какие-то, наоборот, добавляются.
Поэтому прежде чем выбрать такой вариант, необходимо убедиться, что составленная панель отвечает актуальным клиническим рекомендациям, которые можно посмотреть, например, здесь.
Микрочипы
Кроме NGS и ПЦР-исследований есть еще микрочипы. Они позволяют провести скрининг генома, то есть могут «посмотреть» много генов из исследуемого материала и найти известные мутации, ассоциированные с развитием онкологических заболеваний.
Как правило, этот метод используют для скрининга у здоровых людей без отягощенной семейной истории онкологических заболеваний, потому как есть риск пропустить значимую патогенную мутацию.
Обнаружение генетических мутаций, связанных с онкологическими заболеваниями, не означает, что человек точно заболеет раком, но указывает на то, что риск выше среднего.
На основании результатов выбранного исследования врач определит объем и необходимость проведения дополнительных анализов, а также составит персональную программу управления онкологическими рисками.
Кому будет полезен генетический тест?
На самом деле, всем необязательно сдавать генетическое исследование и искать у себя мутации, связанные с возникновением рака любой ценой. Так можно только подогреть канцерофобию. Это тревожное расстройство, когда человек ищет у себя несуществующие симптомы онкологического заболевания и отчаянно пытается проверить всё и сразу, чтобы исключить болезнь.
Но если вы спокойны и просто хотите быть чуть более уверены в этом вопросе, то сдать генетический тест можно.
Вот что вы сможете узнать о раке из генетического теста:
- Какие есть риски развития наследственных заболеваний
В этом случае врач сможет составить индивидуальную программу скрининга по выявленному заболеванию. Такой скрининг может обнаружить рак на ранних стадиях, когда симптомов еще нет. Например, по результатам исследования человеку могут назначить прохождение МРТ молочных желез каждые полгода, если обнаружат патогенные мутации гена BRCA1.
- Как изменить образ жизни, чтобы минимизировать факторы риска
Если человек знает свои наследственные риски, он может начать вести более здоровый образ жизни: избавится от лишнего веса, бросит курить или откажется от алкоголя. Результаты теста помогут найти те факторы, на которые следует обратить внимание в первую очередь.
- Как позаботиться о родных
Информация о патогенной мутации может послужить поводом для проведения генетического тестирования родственникам. Ведь у них тоже может быть повышенный риск развития болезни. В этом случае им понадобится регулярно проходить скрининговые процедуры и изменить свой образ жизни, чтобы снизить свои собственные риски.
Что еще можно узнать о раке из генетического теста?
Например, такие тесты используют для подбора препарата для терапии. Некоторые мутации делают применение ряда химиотерапевтических препаратов неэффективными, а значит пациент может потратить ценное время на бесполезное лечение.
Кроме этого некоторые мутации имеют известные эффекты. Например, они определенным образом меняют структуру белка. Зная это, можно разработать специфические лекарственные препараты, которые будут воздействовать только на опухолевые клетки, не уничтожая нормальные. Эти препараты называют таргетными.
Также некоторые мутации могут указывать на более или менее благоприятный прогноз течения заболевания. Это важно, чтобы выбрать подходящие методы терапии рака.
Узнать больше о том, какие возможности есть у генетических тестов в борьбе с онкологией можно на сайте и у специалистов Центра молекулярной онкологии ОнкоАтлас.
- NIH. The Genetics of Cancer. 2017
- Cancer research UK. Causes of cancer and reducing your risk. 2021
- Myriad. Associated genes and syndroms. 2021
- American cancer society. American Cancer Society Guidelines for the Early Detection of Cancer.
- American cancer society.Family Cancer Syndromes. 2020
- Cross AJ, Ferrucci LM, Risch A, Graubard BI, Ward MH, Park Y, Hollenbeck AR, Schatzkin A, Sinha R. A large prospective study of meat consumption and colorectal cancer risk: an investigation of potential mechanisms underlying this association. 2010
- N.Rahner, V.Steinke. Hereditary Cancer Syndromes.