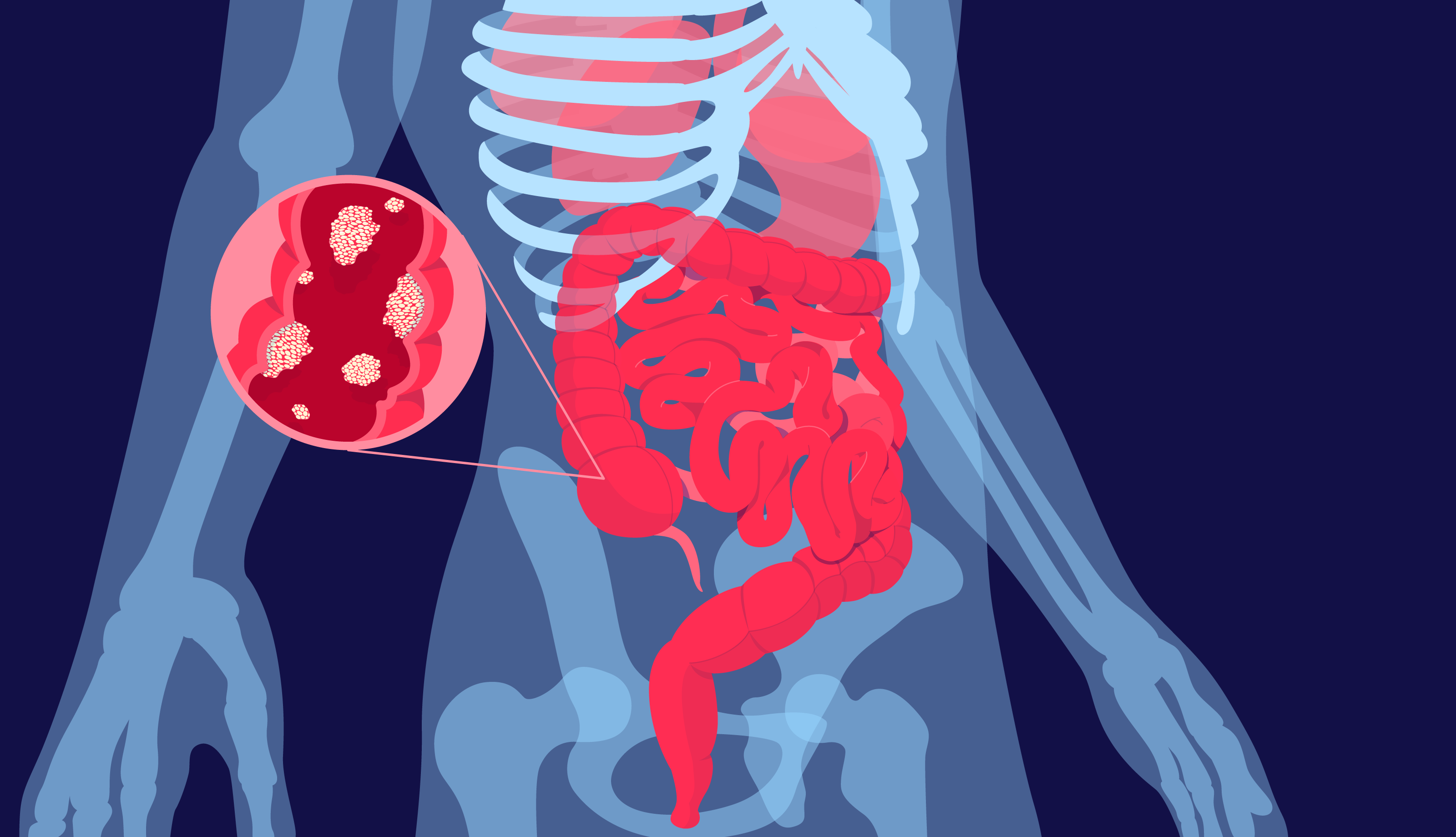
Колоректальный рак — это онкологическое заболевание толстой кишки. В мире колоректальный рак занимает третье место по распространенности среди обоих полов.
Это один из немногих видов рака, для которого есть простые методы ранней диагностики, применяя которые можно выявить болезнь еще на ранней стадии. В этом материале разбираемся в симптомах колоректального рака, его причинах, диагностике и лечении.
Содержание
- Что такое колоректальный рак?
- Какие симптомы появляются при колоректальном раке?
- Почему возникает колоректальный рак?
- Как найти и что делать, если подозреваешь у себя наследственные мутации?
- Можно предотвратить колоректальный рак, если у тебя нет каких-то особых мутаций?
- Как лечат этот тип рака?
Что такое колоректальный рак
При колоректальном раке злокачественные (раковые) клетки образуются в тканях толстой кишки. Это орган пищеварительной системы, который состоит из слепой кишки, ободочной кишки и прямой кишки, которая заканчивается анусом.
Колоректальный рак может возникать из полипов разных типов на слизистой оболочке. Также его вероятность повышает дисплазия, когда в полипе или на слизистой оболочке есть участок, на котором клетки выглядят аномально, но они еще не превратились в опухолевые клетки. Большинство видов рака толстой кишки — это аденокарциномы. Злокачественный процесс в этом случае возникает в клетках железистого эпителия, которые вырабатывают слизь, смазывающую внутреннюю часть толстой кишки.
Какие симптомы появляются при колоректальном раке
Симптомы колоректального рака часто схожи с признаками менее опасных болезней (вроде геморроя или анальной трещины), поэтому появление каких-то из них не значит, что у вас точно рак. Но обратиться к врачу, если заметили какие-то проблемы, необходимо сразу.
Признаки и симптомы, которые должны насторожить:
- кровь в кале, которая возникает регулярно и без очевидной причины;
- изменение работы кишечника, например, появление стойкой диареи или запоров, более частые позывы в туалет;
- постоянная боль внизу живота, вздутие живота или дискомфорт в кишечнике, которые могут сочетаться с потерей аппетита или веса.
Почему возникает колоректальный рак?
Как и другие типы рака, колоректальный рак возникает из-за определенных мутаций в клетках. Некоторые из них возникают случайно в течении жизни человека непосредственно в ткани кишки. Эти мутации невозможно передать детям. Но в некоторых случаях мутации являются наследственными и могут передаваться в семье, а человек получает их с рождения.
К таким состояниям относятся, например, синдром Линча, MutYH-ассоциированный полипоз, синдром Пейтца-Йегерса и семейный аденоматозный полипоз. Обычно наследственные опухолевые синдромы подозревают, если у человека были множественные колоректальные полипы в анамнезе или семейная история колоректальных полипов или рака.
Как найти и что делать, если подозреваешь у себя наследственные мутации?
Специальные генетические тесты могут обнаружить генные мутации, связанные с наследственными синдромами. Например, при семейном аденоматозном полипозе происходят изменения в гене APC, который помогает сдерживать рост клеток. У людей с наследственными изменениями гена APC этот «тормоз» роста отключается.
В результате в толстой кишке образуются сотни полипов, а со временем рак с большой вероятностью разовьется в каком-нибудь из них. При синдроме Линча изменения возникают в генах, которые обычно помогают клетке восстанавливать поврежденную ДНК, — MLH1, MSH2, MSH6, PMS2 и EPCAM. Синдром Пейтца-Егерса вызывается наследственными изменениями гена STK11, а MutYH-ассоциированный полипоз — мутациями в гене MUTYH.
У носителей таких наследственных мутаций существенно меняется программа скрининга и профилактики колоректального рака. Например, при мутации в гене MLH1, колоноскопию советуют начать делать в промежутке от 20 до 25 лет (или на 2-5 лет раньше самого раннего диагноза колоректальный рак в семье, если у родственника он случился до 25 лет), а при мутации в гене MUTYH — с 25-30 лет. Кроме этого, таким пациентам индивидуально могут назначать превентивные операции на кишечнике. Все это нужно, чтобы предотвратить или поймать развитие рака на ранней стадии.
Некоторые наследственные опухолевые синдромы, связанные с развитием колоректального рака, могут увеличивать не только его риск. Так синдром Линча ассоциирован не только с раком толстой кишки, но и с раком яичников, эндометрия, желудка, мочевого пузыря и тонкого кишечника. Поэтому людям с такими мутациями может потребоваться индивидуальный скрининг и этого типа опухолей.
Еще если у людей с наследственными мутациями развивается опухоль в толстой кишке — течение заболевания сильно отличается от обычного колоректального рака и его нужно иначе лечить. Все это показывает, что если у человека есть семейная история колоректальных полипов или рака — очень важно проконсультироваться с генетиком и уточнить, есть ли необходимость генетического тестирования.
Можно предотвратить колоректальный рак, если у тебя нет каких-то особых мутаций?
Людям со средним риском развития колоректального рака (т.е всем остальным в популяции) тоже рекомендуют проводить скрининг, который позволяет обнаружить полипы или злокачественные изменения на ранних стадиях.
Скрининг в разных странах делают чуть по-своему. Врачи могут использовать разнообразные методы: анализ на скрытую кровь в кале, колоноскопию, виртуальную колоноскопию, ДНК-тест кала и другие. Отличается и возраст начала скрининга. Так эксперты Национальной службы здравоохранения Великобритании советуют проходить колоноскопию после положительного теста на скрытую кровь в кале, а начинать скрининг рекомендуют с 50 лет. В США начало скрининга сдвинули на 45 лет, колоноскопию проводят раз в 10 лет, а между ней делают тесты на скрытую кровь в кале.
Как лечат этот тип рака?
Все зависит от стадии рака, но обычно используются методы, что и для других опухолей, вроде химиотерапии, хирургического лечения и лучевой терапии. Отдельно тут можно отметить лечение с помощью таргетной терапии и иммунотерапии.
Во-первых, специалисты обычно проверяют опухоль на наличие мутации в генах KRAS, NRAS или BRAF. Если их нет, пациентам назначают препараты цетуксимаб и панитумумаб. При варианте мутации BRAF V600 цетуксимаб и панитумумаб также могут не работать, но потенциально эффективной терапевтической стратегией тут будет сочетание этих препаратов с ингибиторами BRAF и MEK.
Во-вторых, опухоль могут изучить на микросателлитную нестабильность (MSI) или высокую мутационную нагрузку (TMB, или Tumour Mutational Burden). Таким пациентам можно назначать иммунотерапию, например, пембролизумаб, ниволумаб в монотерапии или в комбинации с ипилимумабом.
Еще при выявлении экспрессии/амплификации HER2 и отсутствии мутаций KRAS/NRAS/BRAF может быть показана анти-HER2 терапия (например, трастузумаб). При выявлении перестроек в таких генах, как NTRK1, NTRK2, NTRK3 можно использовать терапию ингибиторами тирозинкиназ (TRK) — ларотректинибом и энтректинибом.
Узнать больше о генетических рисках развития онкологии или о генетических тестах опухолей можно на сайте и у специалистов Центра молекулярной онкологии ОнкоАтлас.
- World Cancer Research Fund, Colorectal cancer statistics, 2021
- NCCN, Colon Cancer, 2021
- NIH, Colon Cancer Treatment, 2021
- American Cancer Society, What Is Colorectal Cancer?, 2021
- American Cancer Society, What Causes Colorectal Cancer?, 2021
- American Cancer Society, American Cancer Society Guideline for Colorectal Cancer Screening, 2021
- NIH, Genetics of Colorectal Cancer, 2021
- NHS, Bowel cancer, 2021
- Myriad myRisk, MLH1 gene, 2021
- Myriad myRisk, MUTYH Biallelic gene, 2021
- NIH, Colorectal Cancer Screening, 2021
- GOV.UK, Bowel cancer screening: programme overview, 2021